ELEMENTOS BÁSICOS DE FÍSICA NUCLEAR
Es una pequeña región central del átomo donde se encuentran distribuidos los neutrones y protones, partículas fundamentales del núcleo, que reciben el nombre de nucleones.
Para explicar la naturaleza de las fuerzas nucleares que mantienen unidas a las partículas dentro de los núcleos, es necesario analizar sus propiedades. En general, un núcleo tiene una masa y está cargado eléctricamente. Además, tiene un tamaño que se puede medir por su radio. Los nucleones se mueven bajo la acción de sus interacciones mutuas y la intensidad de sus interacciones se puede medir por su energía de enlace o energía de ligadura nuclear.
ΔE = Δm · c2
Donde le llamado “defecto de masa” (Δm ) es igual a la masa de los nucleones menos la masa del núcleo.
La energía de enlace nuclear se define como la energía necesaria para separar los nucleones de un núcleo, o bien como la energía que se libera cuando se unen los nucleones para formar el núcleo.
El origen de la energía de ligadura o de enlace nuclear reside en la desaparición de una parte de la masa de los nucleones que se combinan para formar el núcleo. Esta diferencia de masa recibe el nombre de defecto másico, y se transforma en energía cuyo cálculo se puede realizar por la ecuación de Einstein, E=m.c2
A mayor energía de enlace nuclear más estable será el núcleo.
La descripción básica de la constitución atómica, reconoce la existencia de partículas con carga eléctrica negativa, llamados electrones, los cuales giran en diversas órbitas (niveles de energía) alrededor de un núcleo central con carga eléctrica positiva. El átomo en su conjunto y sin la presencia de perturbaciones externas es eléctricamente neutro.
El núcleo lo componen los protones con carga eléctrica positiva, y los neutrones que no poseen carga eléctrica.
El tamaño de los núcleos atómicos para los diversos elementos está comprendidos entre una cienmilésima y una diezmilésima del tamaño del átomo.
La cantidad de protones y de electrones presentes en cada átomo es la misma. Esta cantidad recibe el nombre de número atómico, y se designa por la letra "Z". A la cantidad total de protones más neutrones presentes en un núcleo atómico se le llama número másico y se designa por la letra "A".
Si designamos por "X" a un elemento químico cualquiera, su número atómico y másico se representa por la siguiente simbología: ZXA
Por ejemplo, para el Hidrogeno tenemos: 1H1.
Si bien, todas las características anteriores de la constitución atómica hoy en día son bastante conocidas y aceptadas, a través de la historia han surgido diversos módelos que han intentado dar respuesta sobre la estructura del átomo. Algunos de tales modelos son los siguientes:
a) El Modelo de Thomson.
Thomson sugiere un modelo atómico que tomaba en cuenta la existencia del electrón, descubierto por él en 1897. Su modelo era estático, pues suponía que los electrones estaban en reposo dentro del átomo y que el conjunto era eléctricamente neutro. Con este modelo se podían explicar una gran cantidad de fenómenos atómicos conocidos hasta la fecha. Posteriormente, el descubrimiento de nuevas partículas y los experimentos llevado a cabo por Rutherford demostró la inexactitud de tales ideas.
b) El Modelo de Rutherford.
Basado en los resultados de su trabajo que demostró la existencia del núcleo atómico, Rutherford sostiene que casi la totalidad de la masa del átomo se concentra en un núcleo central muy diminuto de carga eléctrica positiva. Los electrones giran alrededor del núcleo describiendo órbitas circulares. Estos poseen una masa muy ínfima y tienen carga eléctrica negativa. La carga eléctrica del núcleo y de los electrones se neutralizan entre sí, provocando que el átomo sea eléctricamente neutro.
El modelo de Rutherford tuvo que ser abandonado, pues el movimiento de los electrones suponía una pérdida continua de energía, por lo tanto, el electrón terminaría describiendo órbitas en espiral, precipitándose finalmente hacia el núcleo. Sin embargo, este modelo sirvió de base para el modelo propuesto por su discípulo Neils Bohr, marcando el inicio del estudio del núcleo atómico, por lo que a Rutherford se le conoce como el padre de la era nuclear.
c) El Modelo de Bohr.
El físico danés Niels Bohr ( Premio Nobel de Física 1922), postula que los electrones giran a grandes velocidades alrededor del núcleo atómico. Los electrones se disponen en diversas órbitas circulares, las cuales determinan diferentes niveles de energía. El electrón puede acceder a un nivel de energía superior, para lo cual necesita "absorber" energía. Para volver a su nivel de energía original es necesario que el electrón emita la energía absorbida ( por ejemplo en forma de radiación). Este modelo, si bien se ha perfeccionado con el tiempo, ha servido de base a la moderna física nuclear.
d) Modelo Mecano - Cuántico.
Se inicia con los estudios del físico francés Luis De Broglie, quién recibió el Premio Nobel de Física en 1929. Según De Broglie, una partícula con cierta cantidad de movimiento se comporta como una onda. En tal sentido, el electrón tiene un comportamiento dual de onda y corpúsculo, pues tiene masa y se mueve a velocidades elevadas. Al comportarse el electrón como una onda, es imposible conocer en forma simultánea su posición exacta y su velocidad, por lo tanto, sólo existe la probabilidad de encontrar un electrón en cierto momento y en una región dada en el átomo, denominando a tales regiones como niveles de energía. La idea principal del postulado se conoce con el nombre de Principio de Incertidumbre de Heisenberg, el cual en estricto rigor indica que "variables canónicamentes conjugadas no pueden determinarse simultáneamente con una precisión mejor que  "
"
RADIACIÓN Y RADIOBIOLOGÍA.
RADIOBIOLOGÍA
La radiobiología es la ciencia que estudia los fenómenos que se producen en los seres vivos tras la absorción de energía procedente de las radiaciones ionizantes.
La radiobiología es la ciencia que estudia los fenómenos que se producen en los seres vivos tras la absorción de energía procedente de las radiaciones ionizantes.
Las dos grandes razones que han impulsado la investigación de los efectos biológicos de las radiaciones ionizantes son:
- Protección Radiológica: Poder utilizar esas radiaciones de forma segura en todas las aplicaciones médicas o industriales que las requieran.
- Radioterapia: Utilización de las radiaciones ionizantes principalmente en neoplasias, preservando al máximo los órganos críticos (tejido humano sano).
RADIACIÓN
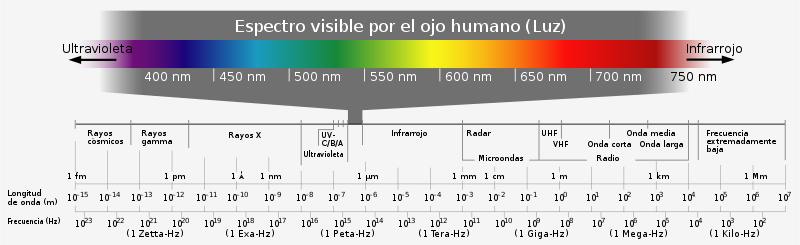
La radiación es la emisión, propagación y transferencia de energía en cualquier medio en forma de ondas electromagnéticas o partículas.
Una onda electromagnética es una forma de transportar energía (por ejemplo, el calor que transmite la luz del sol).
Las ondas o radiaciones electromagnéticas se pueden clasificar en:
- Radiación no ionizante: No tienen la suficiente energía como para romper los enlaces que unen los átomos del medio que irradian (ondas de radio y TV, microondas, luz visible, etc.).
- Radiación ionizante: Tienen suficiente energía como para producir ionizaciones de los átomos del medio o materia que es irradiado. Van desde los rayos X hasta la radiación cósmica.
EFECTOS DE LA RADIACIÓN EN LOS SERES VIVO
Efectos sobre el hombre
Según la intensidad de la radiación y en que parte del cuerpo se produjo, el enfermo puede llegar a morir en el plazo de unas horas a varias semanas. Si sobreviene, sus expectativas de vida quedan sensiblemente reducidas.
Los efectos nocivos de la radiactividad se acumulan hasta que una exposición mínima se convierte en peligrosa después de cierto tiempo. Las condiciones que se expresan cuando alguien es víctima de enfermedad por radiación son:
Ø náuseas
Ø vómitos
Ø convulsiones
Ø delirios
Ø dolores de cabeza
Ø diarrea
Ø pérdida de cabellera
Ø pérdida de dentadura
Ø reducción de los glóbulos rojos en la sangre
Ø reducción de los glóbulos blancos en la sangre
Ø daño al conducto gastrointestinal
Ø pérdida de la mucosa de los intestinos
Ø hemorragias
Ø esterilidad
Ø infecciones bacterianas
Ø cáncer
Ø leucemia
Ø cataratas
Ø daños genéticos
Ø daño cerebral
Ø daños al sistema nervioso
Ø cambio del color de pelo a gris
Ø quemaduras
Ø vómitos
Ø convulsiones
Ø delirios
Ø dolores de cabeza
Ø diarrea
Ø pérdida de cabellera
Ø pérdida de dentadura
Ø reducción de los glóbulos rojos en la sangre
Ø reducción de los glóbulos blancos en la sangre
Ø daño al conducto gastrointestinal
Ø pérdida de la mucosa de los intestinos
Ø hemorragias
Ø esterilidad
Ø infecciones bacterianas
Ø cáncer
Ø leucemia
Ø cataratas
Ø daños genéticos
Ø daño cerebral
Ø daños al sistema nervioso
Ø cambio del color de pelo a gris
Ø quemaduras
ESTRUCTURA Y GENERACIÓN DEL TUBO DE COOLIDGE
En 1913, William Coolidge realizó varias mejoras al tubo de Crookes. El tubo de Coolidge, también conocido como «tubo de cátodo caliente», ha estado en uso desde entonces con algunas modificaciones sobre el diseño básico.
Funciona en un alto vacío, de unos 10−4 Pa, o 10−6 Torr y los electrones son generados por emisión termoiónica en un filamento de wolframio —el cátodo— calentado por una corriente eléctrica. El haz de electrones emitido por el cátodo es acelerado aplicando una diferencia de potencial entre el cátodo y el ánodo; al colisionar con el ánodo, los electrones producen rayos X por los mismos procesos que en el tubo de Crookes.
Tipos
Esquema de un tubo de ánodo rotatorio. A: ánodo; R: rotor; T: área donde incide el haz de electrones; C: cátodo; E: superficie del tubo en vacío; S: estátor; O: volumen ocupado por el aceite refrigerador; B: fuelle que permite la expansión termal del aceite; W: ventana de salida de los rayos X
Ánodo rotatorio
El tubo de ánodo rotatorio es un tubo de Coolidge en el que se hace girar el ánodo mediante inducción electromagnéticagenerada por estátores situados alrededor del tubo. Al girar, el calor generado por el impacto del haz de electrones se distribuye sobre una mayor superficie, lo que permite aumentar la intensidad del haz de electrones en aplicaciones que requieran una alta dosis de rayos X.
Tubos de microfoco
Ciertas técnicas, como la microtomografía, precisan de imágenes de muy alta resolución que pueden conseguirse usando un haz de rayos X de sección reducida. Los tubos de microfoco producen haces con un diámetro típico menor de 50 µm in diameter.
Los tubos de microfoco de ánodo sólido son similares a un tubo de Coolidge convencional, pero con el haz de electrones incide sobre una área muy pequeña del ánodo, normalmente entre 5 y 20 µm; la densidad de potencia del haz de electrones está limitada a un valor máximo de 0.4-0.8 W/µm para no derretir el ánodo, por lo que estas fuentes son poco potentes, por ejemplo, 4-8 W para un haz de electrones de 10 µm de diámetro.
Los tubos de ánodo de metal líquido, en cambio, pueden funcionar con una potencia de 3-6 W/µm. En estos instrumentos, el ánodo sólido es reemplazado por un chorro de metal líquido, generalmente galio en circulación continua. La potencia total es un orden de magnitud mayor que en las fuentes de ánodo fijo, lo que permite disminuir el foco hasta los 5 µm de diámetro, acompañado de una mejora de la resolución de las imágenes y un menor tiempo de exposición.
Cátodo de nanotubos de carbono
El cátodo empleado en los tubos convencionales se puede reemplazar por una serie de nanotubos de carbono que emiten electrones al aplicárseles un voltaje, en vez de por calentamiento, como el filamento de wolframio, por lo que pueden funcionar a temperatura ambiente.
Este diseño fue concebido por un grupo de científicos de la Universidad de Carolina del Norte y patentado en el año 2000. Además de mejorar el consumo de energía, este diseño presenta ventajas en aplicaciones que requieran imágenes de objetos en movimiento: los haces de electrones provenientes de distintos nanotubos emiten rayos X en direcciones distintas, por lo que no es necesario mover el aparato, como ocurre con los tubos con un único filamento, lo que resultaría en imágenes más nítidas.

Aplicaciones en Medicina
Los primeros usos de los tubos de rayos X en medicina y en odontología datan de finales del siglo XIX. Ya los primeros tubos de gas eran empleados para realizar fluoroscopias y radiografías, explotando el contraste en absorción de los rayos X por diferentes tejidos, y se ha documentado su uso en el campo de batalla para localizar balas en soldados heridos.
En la actualidad, también se usan para obtener imágenes médicas tridimensionales mediante la tomografía axial computarizada. Además de su papel como instrumentos de diagnóstico para lesiones óseas, dentales, aflicciones del sistema digestivo y en angiografías, forman parte del equipo usado en algunosprocedimientos quirúrgicos, sobre todo para visualizar la correcta implantación de dispositivos.
Otra aplicación importante, sobre todo en el pasado, fue en el campo de la radioterapia, especialmente en el tratamiento del cáncer y tumores, posible gracias a la capacidad de los rayos X de provocar la muerte celular. Mientras que los tubos de Crookes podían emplearse para tratar tumores superficiales, no fue hasta el desarrollo de los tubos en vacío que se pudo obtener radiación de la suficiente energía para poder alcanzar los tumores internos.
Los tubos de rayos X para esta aplicación requieren un voltaje muy alto y gradualmente han sido reemplazados por otras fuentes de rayos X, como los aceleradores lineales.

PARA MAYOR INFORMACIÓN VISITE: